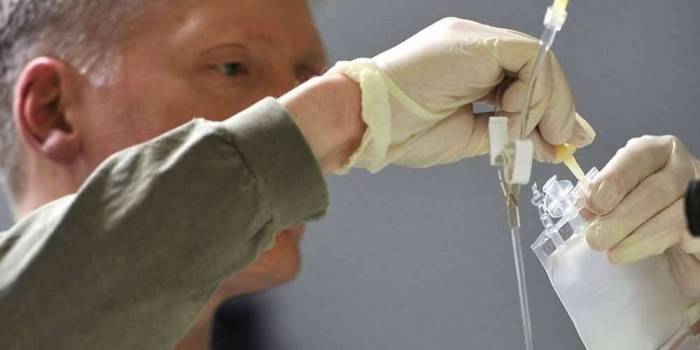
La Commission Européenne a approuvé ce traitement en pédiatrie et pour les jeunes adultes allant jusqu'à 25 ans atteints de leucémie lymphoblastique aiguë à cellules B qui sont réfractaires ou ont fait une rechute après deux autres traitements, a indiqué le groupe bâlois dans un communiqué. "L'homologation de Kymriah est une étape transformatrice pour les patients en Europe qui ont besoin de nouvelles options de traitement," a déclaré Liz Barrett, directrice de Novartis Oncologie, cité dans le communiqué.
Les thérapies géniques sont une nouvelle classe de traitements contre le cancer qui consiste à modifier génétiquement le système immunitaire d'un malade afin il puisse combattre les cellules cancéreuses. Egalement désigné sous le nom de tisagenlecleucel, le Kymriah avait été le premier traitement a recevoir l'autorisation de mise sur le marché par l'agence américaine des médicaments en août l'an passé.
La mise à disposition de ce nouveau traitement dépendra de nombreux facteurs notamment de la présence de personnel formé dans les centres de soins et de la mise en place de procédures de remboursement dans les systèmes nationaux de santé, a précisé Novartis qui est en train de renforcer ses capacités de production pour ce nouveau traitement. Novartis n'a pas donné d'indication sur le prix auquel sera facturé ce nouveau traitement. Jugées très prometteuses, les thérapies géniques ont toutefois soulevé un débat chez les médecins en raison de leurs coûts élevés.



































-1740075441-1744298713.jpg&h=120&w=187&zc=1&q=70')








